martes, 16 de abril de 2013
sábado, 13 de abril de 2013
Hidrocarburos.
El compuesto orgánico más sencillo es el que sólo contiene carbono e hidrógeno y ningún otro elemento; estos compuestos se conocen como HIDROCARBUROS.
Los hidrocarburos se clasifican en:
> ALIFÁTICOS. Son los compuestos orgánicos no derivados del benceno. Están formados por átomos de carbono e hidrógeno, formando cadenas, las cuales pueden ser abiertas o cerradas. Se clasifican en saturados e insaturados.
Los hidrocarburos pueden encontrarse unidos por enlaces simples, dobles o triples llamados alcanos, alquenos y alquinos, respectivamente. Como el carbono es tretavalente, está compartiendo dos electrones en cada enlace (C-C), y el hidrógeno, que solamente tiene un electrón, sólo necesita un enlace para poder juntarse con el carbono.
---->LOS HIDROCARBUROS ALIFÁTICOS PUEDEN SER SATURADOS (ES DECIR, ESTÁN SATURADOS DE HIDRÓGENO) O INSATURADOS (COMPUESTOS QUE TIENEN AL MENOS UN ENLACE DOBLE O TRIPLE ENTRE LOS ÁTOMOS DE CARBONO QUE LOS FORMAN).
 Los alcanos son hidrocarburos formados exclusivamente por carbono e hidrógeno y únicamente hay enlaces covalentes sencillos en su estructura.
Los alcanos son hidrocarburos formados exclusivamente por carbono e hidrógeno y únicamente hay enlaces covalentes sencillos en su estructura.
Fórmula general: CnH2n+2 donde “n” represente el número de carbonos del alcano.
Propiedades y usos de los alcanos.
- El estado físico de los 4 primeros alcanos: metano, etano, propano y butano es gaseoso. Del pentano al hexadecano (16 átomos de carbono) son líquidos y a partir de heptadecano (17 átomos de carbono) son sólidos.
- El punto de fusión, de ebullición y la densidad aumentan conforme aumenta el número de átomos de carbono.
- Son insolubles en agua
- Pueden emplearse como disolventes para sustancias poco polares como grasas, aceites y ceras.
- El gas de uso doméstico es una mezcla de alcanos, principalmente propano.
- El gas de los encendedores es butano.
- El principal uso de los alcanos es como combustibles debido a la gran cantidad de calor que se libera en esta reacción.
+Nomenclatura de los Alcanos.
1.- La base del nombre fundamental, es la cadena continua más larga de átomos de carbono.
2.- La numeración se inicia por el extremo más cercano a una ramificación. En caso de encontrar dos ramificaciones a la misma distancia, se empieza a numerar por el extremo más cercano a la ramificación de menor orden alfabético. Si se encuentran dos ramificaciones del mismo nombre a la misma distancia de cada uno de los extremos, se busca una tercera ramificación y se numera la cadena por el extremo más cercano a ella.
3.- Si se encuentran dos o más cadenas con el mismo número de átomos de carbono, se selecciona la que deje fuera los radicales alquilo más sencillos. En los isómeros se toma los lineales como más simples. El n-propil es menos complejo que el isopropil. El ter-butil es el más complejo de los radicales alquilo de 4 carbonos.
4.- Cuando en un compuestos hay dos o más ramificaciones iguales,no se repite el nombre, se le añade un prefijo numeral. Los prefijos numerales son:
Número
|
Prefijo
|
2
|
di ó bi
|
3
|
tri
|
4
|
tetra
|
5
|
penta
|
6
|
hexa
|
7
|
hepta
|
6.- Se escriben las ramificaciones en orden alfabético y el nombre del alcano que corresponda a la cadena principal, como una sola palabra junto con el último radical. Al ordenar alfabéticamente, los prefijos numerales y los prefijos n-, sec- y ter- no se toman en cuenta.
7.- Por convención, los números y las palabras se separan mediante un guión, y los números entre si, se separan por comas.
La comprensión y el uso adecuado de las reglas señaladas facilitan la escritura de nombres y fórmulas de compuestos orgánicos.

La terminación sistémica de los alcanos es ANO. Un compuestos con esta terminación en el nombre no siempre es un alcano, pero la terminación indica que es un compuesto saturado y por lo tanto no tiene enlaces múltiples en su estructura.
*AlQUENOS (C=C)

Los alquenos son hidrocarburos insaturados que contienen en su estructura cuando menos un doble enlace carbono-carbono.
Formula General: CnH2n
Propiedades y usos de los alquenos.
- Los primeros tres compuestos, eteno (etileno), propeno y buteno, son gaseosos a temperatura ambiente; los siguientes son líquidos hasta los que tienen más de 16 carbonos que son sólidos.
- Son relativamente poco solubles en agua, pero solubles en ácido sulfúrico concentrado y en solventes no polares.
- Su densidad, punto de fusión y de ebullición se elevan conforme aumenta el peso molecular.
- El uso más importante de los alquenos es como materia prima para la elaboración de plásticos.
Nomenclatura de los Alquenos.
Regla 1. Los alquenos son hidrocarburos que responden a la fórmula CnH2n. Se nombran utilizando el mismo prefijo que para los alcanos (met-, et-, prop-, but-....) pero cambiando el sufijo -ano por -eno.
Regla 2. Se toma como cadena principal la más larga que contenga el doble enlace. En caso de tener varios dobles enlaces se toma como cadena principal la que contiene el mayor número de dobles enlaces (aunque no sea la más larga).Regla 3. La numeración comienza por el extremo de la cadena que otorga al doble enlace el localizador más bajo posible. Los dobles enlaces tienen preferencia sobre los sustituyentes.Regla 4. Los alquenos pueden existir en forma de isómeros espaciales que se distinguen con la notación cis/trans.
-En el caso de que hubiera más de un doble enlace se emplean las terminaciones, "-dieno", "-trieno", etc., precedidas por los números que indican la posición de esos dobles enlaces.
La terminación sistémica de los alquenos es ENO.
El más sencillo de los alquenos es el eteno, conocido más ampliamente como etileno, su nombre común.
La mayor parte de los alquenos se obtienen del petróleo crudo y mediante la deshidrogenación de los alcanos.
+ALQUINOS
 Los alquinos son hidrocarburos insaturados que contienen en su estructura cuando menos un triple enlace carbono-carbono.
Los alquinos son hidrocarburos insaturados que contienen en su estructura cuando menos un triple enlace carbono-carbono.
Formula General: CnH2n-2
Propiedades y usos de los alquinos.
- Los tres primeros alquinos son gaseosos en condiciones normales, del cuarto al decimoquinto son líquidos y los que tienen 16 o más átomos de carbono son sólidos.
- La densidad de los alquinos aumenta conforme aumenta el peso molecular.
- Los puntos de fusión y ebullición aumentan con el peso molar de manera similar a los alcanos y alquenos, pero acá resultan ser ligeramente superiores.
- Son poco polares y por lo tanto insolubles en agua, pero muy solubles en benceno, éter y tetracloruro de carbono.
- El etino es el alquino de mayor uso. Es un gas que cuando se quema en presencia de oxigeno puro produce una llama de alrededor de 2800°C, por lo que se utiliza en soldaduras.
- A partir de él también se sintetizan gran cantidad de compuestos orgánicos, siendo el ácido acético uno de los más importantes junto a otros hidrocarburos insaturados capaces de polimerizarse dando plásticos y caucho.
Regla 1. Los alquinos responden a la fórmula CnH2n-2 y se nombran sustituyendo el sufijo -ano del alca-no con igual número de carbonos por -ino.
Regla 2. Se elige como cadena principal la de mayor longitud que contiene el triple enlace. La numera-ción debe otorgar los menores localizadores al triple enlace.
Regla 3. Cuando la molécula tiene más de un triple enlace, se toma como principal la cadena que contie-ne el mayor número de enlaces triples y se numera desde el extremo más cercano a uno de los enlaces múltiples, terminando el nombre en -diino, triino, etc.
Regla 4. Si el hidrocarburo contiene dobles y triples enlaces, se procede del modo siguiente:
1. Se toma como cadena principal la que contiene al mayor número posible de enlaces múltiples, prescindiendo de si son dobles o triples.
2. Se numera para que los enlaces en conjunto tomen los localizadores más bajos. Si hay un doble enlace y un triple a la misma distancia de los extremos tiene preferencia el doble.
3. Si el compuesto tiene un doble enlace y un triple se termina el nombre en -eno-ino; si tiene dos dobles y un triple, -dieno-ino; con dos triples y un doble la terminación es, -eno-diino
En la selección de la cadena más larga, los carbonos que forman triple enlace, siempre deben formar parte de la cadena principal y la numeración se inicia por el extremo más cercano al enlace triple. Al escribir el nombre de la cadena de acuerdo al número de átomo de carbonos, se antepone el número más chico de los dos átomos con el enlace triple y al final se escribe la terminación INO.
>AROMÁTICOS. Los hidrocarburos aromáticos son aquellos hidrocarburos cíclicos que poseen las propiedades especiales asociadas con el núcleo o anillo del benceno (C6H6), en el cual hay seis grupos de carbono-hidrógeno unidos a cada uno de los vértices de un hexágono. Los enlaces que unen estos seis grupos al anillo presentan características intermedias, respecto a su comportamiento, entre los enlaces simples y los dobles. Así, aunque el benceno puede reaccionar para formar productos de adición, como el ciclohexano, la reacción característica del benceno no es una reacción de adición, sino de sustitución, en la cual el hidrógeno es reemplazado por otro sustituto, ya sea un elemento univalente o un grupo.
Presenta cadenas cerradas.
Presenta cadenas cerradas.
+ALÓTROPOS.
A las diferentes estructuras de sustancias con el mismo tipo de átomos se les conoce como
formas alotrópicas.
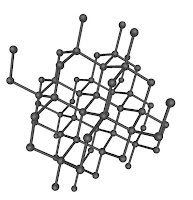
El grafito tiene exactamente el mismo tipo de átomos que el diamante, pero por estar unidos y dispuestos en diferente forma, su textura, fuerza y color son diferentes; sin embargo, la descomposición del diamante es extremadamente lenta que sólo es apreciable a escala geológica.
A las diferentes estructuras de sustancias con el mismo tipo de átomos se les conoce como
formas alotrópicas.
Un ejemplo seria el caso del grafito y el diamante.
 |
| Diamante |
*ISOMEROS
El carbono al unirse a otros átomos de carbono produce una gran variedad de compuestos. A partir de 4 átomos de carbono podemos encontrar dos o más compuestos con la misma cantidad de átomos, en otras palabras, tienen la misma fórmula molecular o condensada, sin embargo, la distribución atómica de éstos es diferente, es decir,sus estructuras no son iguales.
A estos compuestos reciben el nombre de isómeros, que tienen la misma composición atómica pero diferente fórmula estructural, por esto es necesario conocer la fórmula desarrollada o semi desarrollada, para saber qué tipo de compuesto es y poderlo diferenciar del otro, además la estructura podrá ayudar a explicar mejor las propiedades de cada isómero.
Entre mayor sea el número de átomos en un compuesto, mayores son las posibilidades de formar diferentes isómeros, tal como lo muestra la tabla:
Isomería estructural.
-Cadena.
Es la que presentan las sustancias cuyas fórmulas difieren únicamente en la disposición de los átomos de carbono C5H12.
-Posición.
Es la que presenta sustancias cuyas fórmulas estructurales difieren únicamente en la posición de su grupo funcional sobre el esqueleto de carbonos.
-Función.
Es la que presenta sustancias con la misma fórmula molecular teniendo diferente grupo funcional, por ejemplo, C3H6O, puede corresponde a la molécula éter etil-metílico (función éter) o al 2 propanol (función alcohol).
-Función.
Es la que presenta sustancias con la misma fórmula molecular teniendo diferente grupo funcional, por ejemplo, C3H6O, puede corresponde a la molécula éter etil-metílico (función éter) o al 2 propanol (función alcohol).
>RELACIÓN ESTRUCTURA-PROPIEDAD.
Así como las formas alotrópicas del carbono (grafito, diamante, carbono amorfo, fullereno, nanotubos) presentan diferentes propiedades, los isómeros también presentan diferentes propiedades debido a su estructura.
Un ejemplo son los isómeros del C5H12, que como se indica en la tabla, tienen la misma composición, pero diferente estructura. Además de que al aumentar el número de las ramificaciones en la estructura, el punto tanto de ebullición como de fusión se ven afectados.
Esto quiere decir que la estructura que tenga el isómero va a determinar las propiedades físicas y químicas.
Referencias electrónicas.
-http://genesis.uag.mx/edmedia/material/quimicaii/alcanos.cfm#alquenos
-http://quimicaparatodos.blogcindario.com/2009/08/00033-los-alquinos-propiedades-y-usos.html
-http://www.quimicaorganica.org/alquinos/359-nomenclatura-de-alquinos.html
-http://portalacademico.cch.unam.mx/alumno/quimica2/u2/carbono_alimentos/propiedades
-http://www.quimicaorganica.net/nomenclatura-alquenos.html
-http://www.alonsoformula.com/organica/alquinos.htm
-http://portalacademico.cch.unam.mx/alumno/quimica2/u2/carbono_alimentos/isomeria
-http://portalacademico.cch.unam.mx/alumno/quimica2/u2/carbono_alimentos/estructura-propiedad
miércoles, 3 de abril de 2013
El Carbono.
El carbono es un elemento sorprendente no sólo porque existe en diversas formas naturales, como carbono amorfo, diamante y grafito, sino porque sus átomos pueden combinarse entre sí y con átomos de otros elementos para formar millones de compuestos químicos distintos. De hecho, la mayoría de los compuestos químicos en nuestro cuerpo, desde los carbohidratos hasta el ADN y las proteínas son compuestos de carbono. Es por ello que se le considera el elemento de la vida. Su principal compuesto en la atmósfera es el dióxido de carbono (CO2), o también conocido como gas de efecto invernadero.
PROPIEDADES FÍSICAS Y QUÍMICAS DEL CARBONO COMO ELEMENTO.
Una de las propiedades de los elementos no metales como el carbono es por ejemplo que los elementos no metales son malos conductores del calor y la electricidad. El carbono, al igual que los demás elementos no metales, no tiene lustre. Debido a su fragilidad, los no metales como el carbono, no se pueden aplanar para formar láminas ni estirados para convertirse en hilos.
 -PROPIEDADES FÍSICAS: En general son cuerpos sólidos,insoluble en el aguas, son inodoros e insípidos,son mas densos que el agua, a excepción del diamante, son de color negro, frágiles y untuosos al tacto. El carbono se encuentra en las formas carbón, grafito, diamante, fullereno y nanotubos. Éstos son materiales con propiedades muy diferentes, pero a nivel microscópico sólo difieren por las disposiciones geométricas de los átomos de carbono.
-PROPIEDADES FÍSICAS: En general son cuerpos sólidos,insoluble en el aguas, son inodoros e insípidos,son mas densos que el agua, a excepción del diamante, son de color negro, frágiles y untuosos al tacto. El carbono se encuentra en las formas carbón, grafito, diamante, fullereno y nanotubos. Éstos son materiales con propiedades muy diferentes, pero a nivel microscópico sólo difieren por las disposiciones geométricas de los átomos de carbono.
-PROPIEDADES QUIMICAS
El carbono y sus compuestos
se encuentran distribuidos ampliamente en la naturaleza. Se estima que el
carbono constituye 0.032% de la corteza terrestre. El carbono libre se
encuentra en grandes depósitos como hulla, forma amorfa del elemento con
otros compuestos complejos de carbono-hidrógeno-nitrógeno. El carbono
cristalino puro se halla como grafito y diamante.
|
Número
atómico
6
Valencia
4
Grupo
14
Periodo
2
2,+4,-4
Estado de oxidación
+4
Electronegatividad
2,5
Radio covalente (Å)
0,77
Radio iónico (Å)
0,15
Radio atómico (Å)
0,914
Configuración electrónica
1s22s22p2
Primer potencial de ionización (eV)
11,34
Masa atómica (g/mol)
12,01115
Densidad (g/ml)
2,26
Punto de ebullición (ºC)
4830
Punto de fusión (ºC)
3727
Óxido
Ácido fácil
Estructura cristalina
Hexagonal
Tipo de
enlace
Covalente
(puro, no polar y polar)
Presenta 3 tipos de enlace:
Enlace simple C-C
Enlace doble C=C
Enlace
triple C---C
VÍDEO DEL CARBONO.
El Carbono en la Naturaleza
Compuestos Orgánicos del Carbono
PROPIEDADES FÍSICAS.
ALOTROPO
|
PUNTO
DE FUSIÓN
|
PUNTO
DE EBULLICIÓN
|
DENSIDAD
|
CONDUCTIVIDAD
|
ESTADO FISICO
|
SOLUBILIDAD
|
DUREZA
|
ESTRUCTURA
|
USOS
|
|
Fullereno
|
3800
K
|
5100
K
|
1,68 g/cm3
|
0,7 (mOhm.cm)-1
|
Solido
de color negro
|
Es
insoluble.
|
0,8
(grafito)
|
-Imitación del diamante
-Catalizadores -Productos cosméticos -Los superconductores -Agente abrasivo para cortar y moler aplicaciones. -Colorantes y pigmentos -Electrodos -Aditivo lubricante -Antioxidante para usos medicinales -Los antibióticos a bacterias diana -Contra el cáncer de algunos tipos de células -Polímeros fotoactivos |
||
Nanotubos de carbono
|
1.33 a 1.40 g/cm3
|
Son buenos conductores
|
Soluble
|
Son muy duros (similares a los diamantes).
|
-Inmunoquimica
-Pipetas moleculares -Sensores de ADN -Rayos X a temperatura normal -Tratamiento contra el cáncer -Nanoelectrónica -Pantallas planas -Memoria mecánica -Sensores de gases -Almacenamiento electroquímico de energía -Pilas de combustible -Plásticos conductores -Nuevos materiales de carbono |
|||||
Carbono
Amorfo
|
3.925 °C
|
3000 °C
|
2,25 kg/m3
|
Es buen conductor .
|
Solido
|
Soluble
|
Es muy duro y resistente
|
-componente de hidrocarburos, especialmente de los
combustibles fósiles (petróleo y gas
natural).
Petróleo: gasolinas, aceites, plásticos. -aditivo para el acero en las construcciones -gas natural: fuente limpia de combustión |
||
| Alta |
----
|
2,09 a 2,23 g/cm3
|
Excelente conductor
|
Solido
|
Es soluble
|
Es muy resistente
|
||||
Diamante
|
3823 °C
|
4827 °C
|
3,5-3,53 g/cm3
|
Es semiconduc-tor
|
Solido
|
Es insoluble
|
Es duro.
|
-Se utiliza en
aplicaciones de joyería e industriales.
|
PROPIEDADES QUÍMICAS.
Compuestos Inorgánicos
Compuestos Inorgánicos
>Sales Binarias: Carburo de Litio (Li4C)
Carburo de Berilio (Be2C)
Carburo de Magnesio (Mg2C3)
Carburo de Calcio (CaC2)
Carburo de Boro (B4C)
>Sales Terciarias: Carbonato de Calcio (CaCO3)
Carbonato de Sodio (Na2CO3)
Carbonato de Potasio (K2CO3)
Carbonato de Zinc (ZnCO3)
Carbonato de Bario (BaCO3)
>Cianuros: Cianuro de Potasio (KCN)
Cianuro de Sodio (NaCN)
Cianuro de Calcio (CaCN2)
>Ácidos: Oxiácido---> ácido carbónico (H2CO3)
ácido carbonoso (H2CO2)
>Óxidos: Dióxido de Carbono (CO2)
Monoxido de carbono (CO)
Tetroxido de Carbono (CO4)
Compuestos Orgánicos
Hidrocarburos.
Los compuestos orgánicos mas simples son los hidrocarburos, los cuales contienen solo los elementos carbono e hidrógeno (HC). Los Hidrocarburos se clasifican en:

-->ALIFÁTICOS.
Son HC de cadenas abiertas o cerradas y se clasifican en saturados e insaturados dependiendo de la cantidad de átomos de hidrógeno y está determinado por las uniones carbono-carbono, simples, dobles y triples llamados alcanos, alquenos y alquinos respectivamente.
 --->ALCANOS.(C-C) El metano es el miembro mas pequeño de una serie de hidrocarburos conocida como alcanos. Los alcanos tienen solo enlaces simples entre los átomos Son HC saturados, cuya formula es: CnH2n+2, para cadenas abiertas, ya sean lineales o ramificadas; pero si la estructura es cíclica la formula es: CnH2n.
--->ALCANOS.(C-C) El metano es el miembro mas pequeño de una serie de hidrocarburos conocida como alcanos. Los alcanos tienen solo enlaces simples entre los átomos Son HC saturados, cuya formula es: CnH2n+2, para cadenas abiertas, ya sean lineales o ramificadas; pero si la estructura es cíclica la formula es: CnH2n.
Carburo de Berilio (Be2C)
Carburo de Magnesio (Mg2C3)
Carburo de Calcio (CaC2)
Carburo de Boro (B4C)
>Sales Terciarias: Carbonato de Calcio (CaCO3)
Carbonato de Sodio (Na2CO3)
Carbonato de Potasio (K2CO3)
Carbonato de Zinc (ZnCO3)
Carbonato de Bario (BaCO3)
>Cianuros: Cianuro de Potasio (KCN)
Cianuro de Sodio (NaCN)
Cianuro de Calcio (CaCN2)
>Ácidos: Oxiácido---> ácido carbónico (H2CO3)
ácido carbonoso (H2CO2)
>Óxidos: Dióxido de Carbono (CO2)
Monoxido de carbono (CO)
Tetroxido de Carbono (CO4)
Compuestos Orgánicos
Hidrocarburos.
Los compuestos orgánicos mas simples son los hidrocarburos, los cuales contienen solo los elementos carbono e hidrógeno (HC). Los Hidrocarburos se clasifican en:

-->ALIFÁTICOS.
Son HC de cadenas abiertas o cerradas y se clasifican en saturados e insaturados dependiendo de la cantidad de átomos de hidrógeno y está determinado por las uniones carbono-carbono, simples, dobles y triples llamados alcanos, alquenos y alquinos respectivamente.
-->AROMÁTICOS
Son Hidrocarburos cíclicos en donde el benceno es un liquido incoloro e inflamable que se obtiene sobre todo en le petroleo y el alquitrán reactiva.
--->HIDROCARBUROS SATURADOS
Son aquellos compuestos que tienen el máximo de átomos de hidrógeno en su estructura molecular. Estos compuestos solamente se presentan en enlaces simples: C-C o C-H.
Son aquellos compuestos que tienen el máximo de átomos de hidrógeno en su estructura molecular. Estos compuestos solamente se presentan en enlaces simples: C-C o C-H.
--->HIDROCARBUROS INSATURADOS.
Son aquellos compuestos que tienen al menos un enlace doble o triple entre los átomos de carbono que los forma. La cantidad de átomos de hidrógeno que tiene los HC insaurados es menor a la de los saturados de igual numero de átomos de carbono.
---->HIDROCARBUROS LINEALES.Es una cadena de átomos de carbono (C) unidos entre sí con enlaces sencillos, dobles o triples. Es posible que un cierto átomo de carbono no use todos sus enlaces posibles (un total de 4) para unirse a otros átomos de carbono. En este caso, los enlaces restantes se hacen con átomos de hidrógeno (H). Un hidrocarburo lineal se puede especificar por la secuencia de enlaces.
--->HIDROCARBUROS RAMIFICADO.
La cadena de mayor numero de átomos de carbono es considerada como la cadena principal y las cadenas adicionales se consideran ramificadas. En un HC cíclico toda cadena adicional a este se considera ramificación.
 --->ALCANOS.(C-C) El metano es el miembro mas pequeño de una serie de hidrocarburos conocida como alcanos. Los alcanos tienen solo enlaces simples entre los átomos Son HC saturados, cuya formula es: CnH2n+2, para cadenas abiertas, ya sean lineales o ramificadas; pero si la estructura es cíclica la formula es: CnH2n.
--->ALCANOS.(C-C) El metano es el miembro mas pequeño de una serie de hidrocarburos conocida como alcanos. Los alcanos tienen solo enlaces simples entre los átomos Son HC saturados, cuya formula es: CnH2n+2, para cadenas abiertas, ya sean lineales o ramificadas; pero si la estructura es cíclica la formula es: CnH2n.
--->ALQUENOS.(C=C) Son HC insaturados con doble ligadura, ya que en su molécula tienen cuando menos 2 átomos de carbono unidos por un doble enlace. El eteno es el primer miembro de esta familia. Su formula es: CnH2n, para cadenas abiertas, ya sea lineales o ramificadas.
--->ALQUINOS. (C---C) Dos átomos de carbono también pueden compartir 3 pares de electrones para formar un triple enlace entre los 2 átomos de carbono, como en el etino C2H2. Son HC insaturados y su formula es: CnH2n-2, para cadenas abiertas, ya sea lineales o ramificadas.
Bibliografias.
https://sites.google.com/a/uji.es/alotropos-del-carbono/bu
http://portalacademico.cch.unam.mx/alumno/quimica2/u2/carbono_alimentos/propiedades
http://www.uam.es/docencia/elementos/spV21/sinmarcos/elementos/c.html
http://elperiodicoquimico.galeon.com/album1462472.html
http://www.lenntech.es/periodica/elementos/c.htm
http://www.fullquimica.com/2012/08/propiedades-fisicas-del-carbono.html
http://elementos.org.es/carbono
http://es.scribd.com/doc/31259660/Cianuro
-RICO, Galicia Antonio; PEREZ, Orta Rosa Elba
"Quimica. Segundo curso para estudiantes del Bachillerato del CCH"
Colegio de Ciencias y Humanidades
México,2012
p.p 143,144,145,154
->MEISLICH, Ph. D. Herbert
“Química Orgánica”
2° edición
Mc Graw-Hill
España, 1993
p.p. 59,60,104,115,171,172.
QD257
M4318
1991
2° edición
Mc Graw-Hill
España, 1993
p.p. 59,60,104,115,171,172.
QD257
M4318
1991
>DINGRANDO,
Laurel.
“Química. Materia y Cambio”
Mc Graw-Hill
Colombia, 2002
p.p. 698,699,700,701,709,711,712.
QD31
.3
C4418
“Química. Materia y Cambio”
Mc Graw-Hill
Colombia, 2002
p.p. 698,699,700,701,709,711,712.
QD31
.3
C4418
Suscribirse a:
Comentarios (Atom)